«Ich glaube an die Präzisionsmedizin»
Marianna Kruithof-de Julio und ihr Team entwickeln Methoden, um aus Tumorbiopsien kleine Zellhaufen zu züchten. Damit wollen die Forschenden die Behandlung massgeschneidert auf jede Patientin und jeden Patienten ausrichten. Ihr Ziel sei vielleicht noch fünf bis zehn Jahre entfernt, schätzt die Expertin.

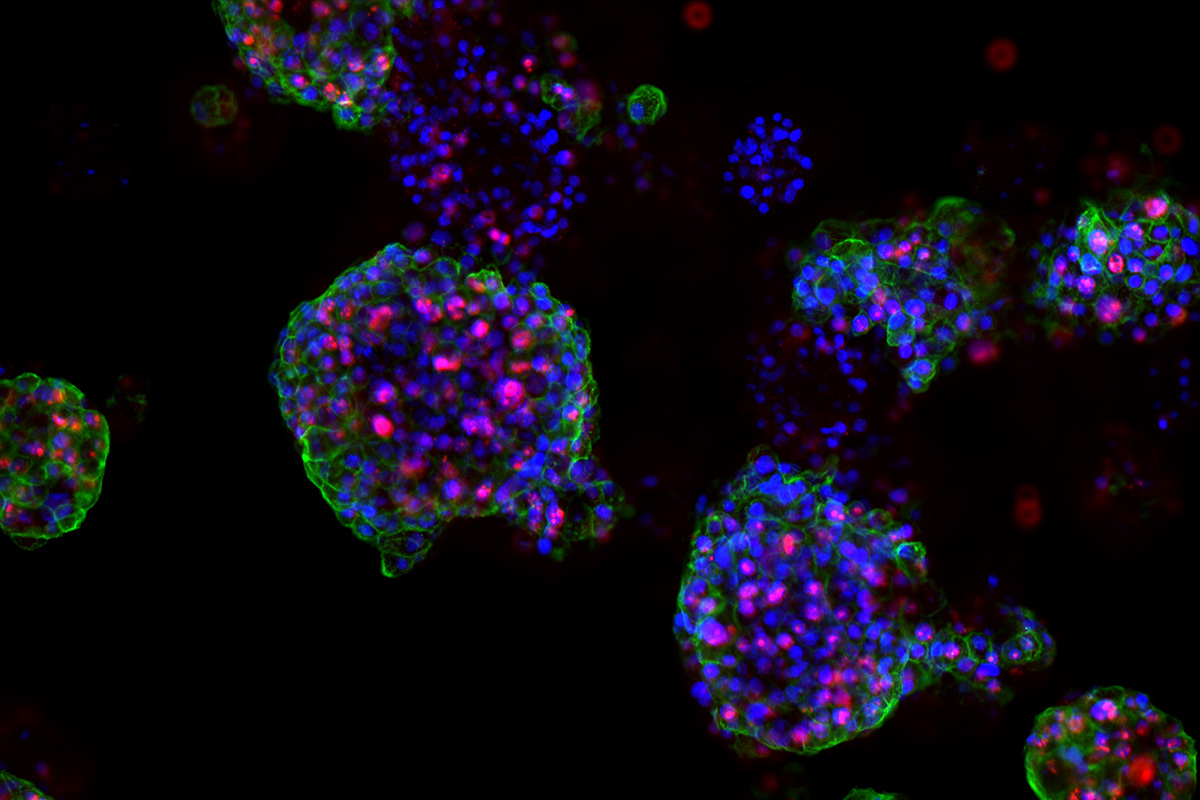
Marianna Kruithof-de Julio: Wir entwickeln Methoden, um aus biologischen Proben von Krebspatientinnen und -patienten Zellen züchten und vermehren zu können. Wir versuchen dabei, günstige Bedingungen für die Zellen zu schaffen, so dass sie sich zu kugelförmigen Zellhaufen – sogenannten Organoiden – zusammenschliessen. Diese Organoide sind ein ziemlich präzises Abbild des Tumors, aus dem sie gezüchtet wurden. Die Unterschiede zwischen den Patientinnen und Patienten können wir weder mit herkömmlichen Zelllinien noch mit Tiermodellen so gut nachahmen. Aktuell sind wir damit beschäftigt, die Verfahren zu optimieren und zu standardisieren, damit wir die patientenspezifischen Organoide in breiten Tests verwenden können.
Wozu?Um für jede Patientin und jeden Patienten einzeln testen zu können, welche Medikamente am wirksamsten sind. Im Moment noch machen wir das allerdings nur bei Fällen, in denen die Medizin nicht mehr weiter weiss, weil der Tumor Resistenzen gegen die Standardbehandlung entwickelt hat. Wir tragen also erst am Schluss des Patientinnen- oder Patientenpfads zur klinischen Entscheidungsfindung bei. Meine Vision ist, dass wir schon am Anfang beigezogen würden. Die Pathologinnen und Pathologen würden das Biopsiematerial gleich zu Beginn aufteilen. Sie würden nach wie vor den Tumor diagnostizieren und charakterisieren, parallel dazu könnten wir die Organoide züchten. Wenn die Bioinformatik weiterhin solche rasanten Fortschritte macht, lässt sich meine Vision vielleicht schon in fünf bis zehn Jahren verwirklichen.
Ja, doch was wir in der Studie am Beispiel von fünf Patienten mit Prostatakrebs durchgespielt haben, können wir so noch nicht auf den klinischen Alltag übertragen. Denn noch sind die Abläufe nicht richtig eingespielt – und der Koordinationsaufwand dementsprechend hoch. Aber ich glaube an die Präzisionsmedizin. Wenn wir die Behandlung auf die individuellen Merkmale eines Tumors ausrichten können, erzielen wir in vielen Fällen bessere Resultate. In Zukunft wird der Krebs immer seltener eine tödliche und dafür immer öfter eine chronische Erkrankung sein. Doch um aus der Utopie eine Realität zu machen, müssen wir Forschenden Hand in Hand mit den Klinikerinnen und Klinikern zusammenarbeiten. Um den engen und sehr guten Austausch mit Professor George Thalmann und seinen Mitarbeitenden an der Universitätsklinik für Urologie des Inselspitals Bern bin ich deshalb froh und dankbar.
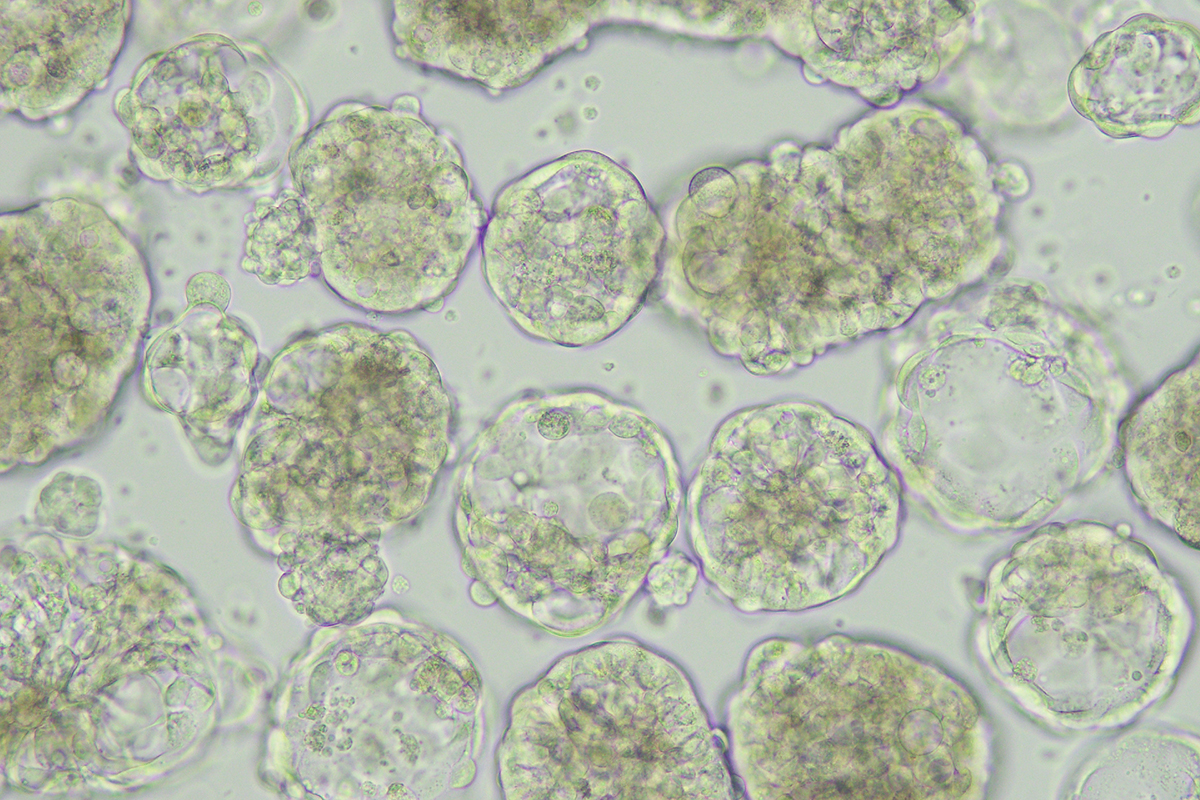
Organoide ermöglichen die Untersuchung biologischer Prozesse, wie Zellverhalten, Gewebereparatur und Reaktion auf Medikamente oder Mutationen, in einer Umgebung, die die körpereigene Zellorganisation und Organstrukturen nachahmt. Organoide haben sich von einem ursprünglichen Durchbruch in der Technologie mittlerweile als unverzichtbares Werkzeug in der biologischen Forschung etabliert und sind auch für die klinische Anwendung von Bedeutung. Zu den wichtigsten Vorteilen gehört, dass sie aus einem begrenzten Vorrat an Ausgangsmaterial, zum Beispiel Biopsien, gezüchtet werden können; das schnelle Wachstum im Vergleich zu sogenannten PDX-Modellen (patient-derived xenografts), wobei Gewebebiopsien von Patientinnen und Patienten in ein Tiermodell – in diesem Fall Mäuse – transferiert werden. Weitere Vorteile sind das Potenzial, 3D-Wachstum zu modellieren und dass man sie mit Gen-Editing-Tools wie CRISPR-cas9 bearbeiten kann, um Modellsysteme mit ähnlicher Komplexität zu schaffen, wie sie in einer Population von Krebspatientinnen und Krebspatienten vorkommen; die direkte Anwendung auf das Präzisions-Onkologie-Management, um die nächsten oder besten Therapien zu antizipieren – all dies wird dazu führen, dass der Bedarf an Tierversuchen dank Organoiden deutlich sinken wird.
Medienmitteilung
Zur Person

PD Dr. Marianna Kruithof-de Julio ist seit 2016 Forschungsgruppenleiterin am Department for BioMedical Research (DBMR) und am Bern Center for Precision Medicine (BCPM) der Universität Bern und des Inselspitals. Ihr Forschungsschwerpunkt liegt in der Entwicklung und Anwendung von Werkzeugen für die Präzisionsmedizin. In den letzten Jahren hat sie mehrere hochkompetitive Grants eingeworben, etwa vom «Congressionally Directed Medical Research Program» (CDMRP) der USA und vom 3R Kompetenzzentrum Schweiz (3RCC).
Kontakt:
PD Dr. Marianna Kruithof-de Julio
Urologie-Forschungslabor am Department for BioMedical Research (DBMR) und Bern Center for Precision Medicine (BCPM), Universität Bern und Inselspital Bern
Telefon: +41 31 632 09 31 / marianna.kruithofdejulio@dbmr.unibe.ch
Über den Autor
Ori Schipper ist Science Writer. Er lebt und arbeitet in Bern.