Neuartige Therapie gegen Angst- und Stresserkrankungen
Synendos, ein Spin-off der Universität Bern und des Nationalen Forschungsschwerpunkts TransCure, entwickelt eine Therapie für angst- und stressbedingte Erkrankungen. Für erste klinische Tests erhält Synendos 20 Millionen Franken von Pharma-Investoren. Ein Interview mit Co-Gründer Jürg Gertsch.

Für mich persönlich, aber auch für das ganze Forschungsteam, ist es ein grosser Erfolg. Aus einer anfänglichen Idee und der Grundlagenforschung könnte nun ein neues Medikament werden. Diese Finanzierung ermöglicht den entscheidenden Schritt in Richtung klinischer Entwicklung unseres Arzneistoffs. Nun wird sich zeigen, ob unsere Therapie auch beim Menschen wirkt. Es ist 25 Jahre her, dass ein Medikament mit einem neuen Wirkungsmechanismus für die Behandlung von neuropsychiatrischen Erkrankungen zugelassen wurde. Es ist also höchste Zeit für neue Therapieansätze. Wir freuen uns sehr, dass wir mit unserer neuen Technologie eine so starke internationale Gruppe von Investoren überzeugen konnten.

Arzneimittel können wegen der enorm hohen Entwicklungskosten nicht an Universitäten entwickelt werden. Dies erfordert grosse Investitionen aus Privat- oder Risikokapital und später die Zusammenarbeit mit grossen Pharmaunternehmen. Synendos wird zunächst die vollständige toxikologische Bewertung der von uns entwickelten Technologie abschliessen – also abklären, ob sie sicher ist. Erst dann kann sie am Menschen getestet werden. Mit der Summe werden erste klinischen Studien am Menschen finanziert, wobei der Schwerpunkt zunächst auf neuropsychiatrischen Erkrankungen liegt, für die es bislang keine ausreichend wirksamen pharmakologischen Therapien gibt.
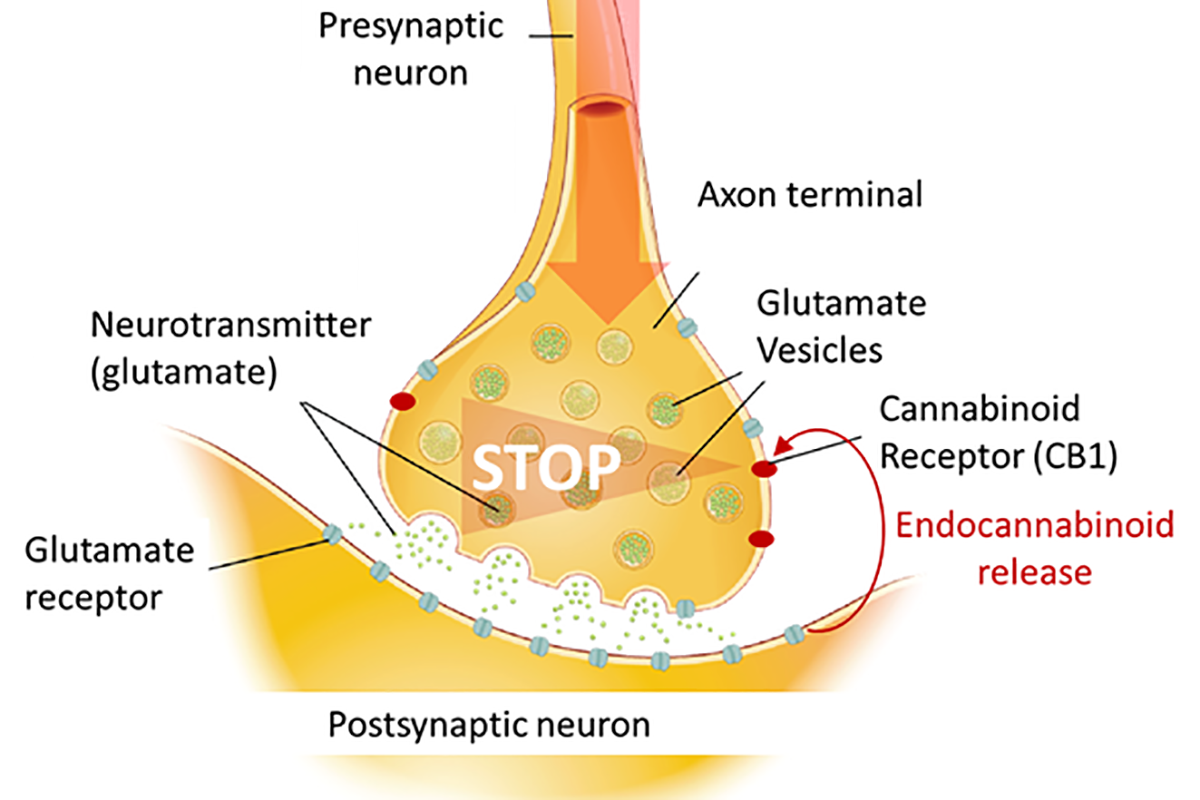
Worin besteht die Innovation Ihres Ansatzes?Das Endocannabinoid-System ist ein biochemisches System in unserem Körper, das auf Stress reagiert. Dabei hemmen körpereigene Cannabinoide, also Endocannabinoide, Signale von Nervenzellen. Das Endocannabinoidsystem ist grundlegend, um das Gehirn im Gleichgewicht zu halten. In unserem Labor haben wir die biologischen Grundlagen für den Transport von Endocannabinoiden durch die Zellmembran entdeckt. Darauf basierend entwickelten wir Stoffe, die diesen Transport blockieren. Dies hat enorme Vorteile gegenüber bisherigen Methoden, die versuchen, das Endocannabinoid-System zu beeinflussen: So können zwar die Endocannabinoid-Rezeptoren durch externe Verbindungen wie den Cannabinoiden, beispielsweise THC, direkt aktiviert werden, was jedoch zu schweren Nebenwirkungen führen kann. Oder man kann die Enzyme hemmen, die Endocannabinoide abbauen, und das System so wiederherstellen – dieser Ansatz wird von vielen Pharmaunternehmen weltweit verfolgt. Ein möglicher Nachteil dieses Mechanismus könnte jedoch sein, dass zu viele Endocannabinoide produziert werden.
Genau hier setzen wir an: Wir verwenden sogenannte selektive Endocannabinoid-Wiederaufnahmehemmer, die eine zu hohe Wiederaufnahme und den Abbau von Endocannabinoiden verhindern, ohne jedoch zu einer Überproduktion zu führen. Ein überaktiver Abbau von Endocannabinoiden wird häufig bei neuropsychiatrischen Erkrankungen wie der posttraumatischen Belastungsstörung (PTBS) beobachtet. Eine Überproduktion von Endocannabinoiden wiederum kann zu metabolischen und kardiovaskulären Schäden führen. Die Technologie der sogenannten SERIs (selective endocannabinoid reuptake inhibitors) wird nun von der Startup-Firma Synendos Therapeutics weiterentwickelt, mit dem Ziel, neuropsychiatrische Störungen im Zusammenhang mit Angst und Stress zu behandeln.
Sehr gross. Die meisten der heute angewandten Therapien gehen immer noch auf Erkenntnisse des letzten Jahrhunderts zurück. Dabei wird die Translation, also das «Übersetzen» von Forschungsergebnissen in klinische Produkte oder Therapien, oft durch die mangelnde Reproduzierbarkeit von Tierversuchen am Menschen behindert. Gegenwärtig gibt es zum Beispiel zwar Psychotherapien, aber keine Pharmakotherapie für eine PTBS – eine psychische Erkrankung, die zu lebenslangen Behinderungen führen kann. PTBS betrifft zwischen einem und acht Prozent der Weltbevölkerung und weist bei Frauen höhere Raten auf. Einige PTBS-Patientinnen und -Patienten können aufgrund starker traumatischer Erinnerungen nicht mit einer Psychotherapie behandelt werden. Das Endocannabinoid-System ist entscheidend an der lebensnotwendigen Löschung stark unangenehmer Erinnerungen beteiligt, und wir glauben daher, dass die Wiederherstellung dieses Systems gerade solche stressvollen Erinnerungen unterdrücken kann.
Synendos Therapeutics ist im Rahmen des NFS TransCure entstanden, in dem Sie auch tätig sind. Was können Forschungsnetzwerke tun, um die Translation zu unterstützen?Sie können die transdisziplinäre Vision der Forschung fördern und Menschen aus sehr unterschiedlichen Disziplinen zusammenbringen, um am gleichen Problem zu arbeiten. Es geht nicht nur um Forschungsarbeiten, sondern auch darum, Wissen zu nutzen, um Probleme zu lösen. Wir tun dies derzeit im NFS TransCure mit einem neuen Projekt, in dem Chirurgen, Pharmazeutinnen und Chemiker zusammenarbeiten. Ich finde das sehr spannend.
Zur Person

Prof. Dr. Jürg Gertsch ist seit 2014 Professor für Biochemie an der Universität Bern. Zurzeit ist er Ordinarius für Pharmazeutische Biologie und Co-Direktor des Instituts für Biochemie und Molekulare Medizin sowie Mitglied des Nationalen Forschungsschwerpunktes TransCure. Seit mehr als zehn Jahren untersucht seine Forschungsgruppe das Endocannabinoid-System mit verschiedenen analytischen, chemisch-biologischen und pharmakologischen Ansätzen.
Kontakt:
Prof. Dr. Jürg Gertsch
Institut für Biochemie und Molekulare Medizin und NFS TransCure, Universität Bern
+41 31 631 41 24 / juerg.gertsch@ibmm.unibe.ch
Nationaler Forschungsschwerpunkt (NFS) TransCure
Der NFS TransCure ist ein interdisziplinäres, schweizweites Netzwerk von 15 Forschungsgruppen, finanziert vom Schweizerischen Nationalfonds und mit der Universität Bern als Heiminstitution. Im Zentrum des Netzwerks steht die Forschung auf dem Gebiet des Membrantransports und der Ionenkanäle. Diese dienen als «Türwächter», die den Transport von Nährstoffen, Medikamenten und anderen Substanzen durch die Zellmembran ermöglichen. Eine Fehlfunktion der Transporter kann zu häufigen und seltenen menschlichen Krankheiten wie neurologischen und kardialen Störungen, Diabetes, Osteoporose und Krebs führen. Die NFS TransCure-Projekte zeichnen sich durch eine einzigartige Kombination von drei Disziplinen – aus Physiologie, Chemie und Strukturbiologie – und umfassen sowohl Grundlagen- als auch vorklinische Forschung.
Zur Autorin
Nathalie Matter ist Redaktorin und Themenverantwortliche für Gesundheit und Medizin in der Abteilung Kommunikation & Marketing der Universität Bern.